Text
نشأة الكيمياء الضوئية بدأ من القانون الأول لها والذي نصه ( Grotthuss &Draper ) حيث يقول بأن الضوء الممتص من قبل المادة هو المسؤول عن التغير الكيميائي الحاصل لها !/ لتصبح الحجر الأساس لفهم التفاعل الكيميائي الناتج من تواجد ضوء.

ثم يأتيان كلاً من ( Stark & Einstein ) لينصا القانون الثاني وهو أن الضوء عبارة عن فوتونات .. كل جزيء من المادة يمتص فوتون واحد ولكن ليتم ذلك لابد يكون له طاقة محددة تساهم في حدوث التفاعل لذلك ١ مول من جزيئات المادة المثارة يمتص ١ مول من الفوتونات على إفتراض أن جميع ال١ مول تفاعل

Beer & Lambert وصفوا شدة إمتصاص الضوء من قِبل المادة بأنها ثابت أسمه معامل الإمتصاصية وهو يختلف حسب كل مادة فإذا كانت المادة لها معامل إمتصاص عالي فإن إمتصاصها سيظهر عند تراكيز منخفضة مثل البرمنجنات. لذلك اللوغاريثم لشدة الاشعة الممتصة على الأشعة المسلطة يعبر عنه بالإمتصاصية A وهي على علاقة طردية بالتركيز
Log Io/I = A = ε l c
يأتي بعد ذلك مبدأ ( Frank - Condon ) والذي ينص على أن الضوء المسلط على جزيء أو ذرة يؤثر بشكل مباشر على الإلكترون وليس النواة على فرض أن النواة ذات كتلة ضخمة مقارنة بالالكترون لذلك فهي ثابتة والتأثير كله يقع على الالكترون تحت ٣ طاقات .. إنتقالية و إهتزازية و دورانية والانتقالية تعتبر الأعلى ثم الاهتزازية فالدورانية.
هناك ٦ إنتقالات الكترونية و الإنتقالات التي تحصل من σ إلى σ*, π*, n ليست ذات أهمية كونها تحتاج أطوال موجية منخفضة جداً والتركيز يصب على الإنتقالات *π —> π و
n —> π*
وهي المسؤولات عن التفاعلات الكيميائية العضوية.
في بدايات الكيتونات و الالدهيدات أول المركبات التي تمت دراستها من قبل نوريش وحصل عليها نوبل عام ١٩٦٧ .. درس نوريش التكسير الضوئي لهذه المركبات و وضع نوعين منهم وضعت بأسمه
Norrish type I
وفيها تحصل إثارة للكربونيل فتنكسر الرابطة بين الكربونيل و الكربون ألفا ( α-cleave ) معدل التكسير يعتمد على ثباتية الجذر المتكون في الكربون الفا .. فتكوت النتيجة عادةً خروج أول اكسيد الكربون و الحصول على جذريين كربون حرة
Norrish type II
وفيها تحصل إثارة الكربوني�� فيقوم الاكسجين بنزع الهيدروجين في موقع γ قبل الحصول على النواتج
من مشاكل هذا النوعيين من التفاعل أن النواتج تكون خليط وليس ناتج واحد محدد لكنها دراسات ممتازة ومفيدة لفهم طبيعة هذه التفاعلات
طالما الحديث يطال الانتقالات الإلكترونية فلابد الأخذ بعين الإعتبار ما يُسمى بالمغزلية التعددية ( Spin multiplicity ) والمُعطى بالمعادلة
Spin multiplicity = 2S+1
الحالة المغزلية في مركبات العضوية تتواجد الكتروناتها إما في الحالة الأُحادية Singlet وهذا يكون عندما تكون مغزلية الإلكترونيين عكس بعضهم ( +1/2 & -1/2 )
Spin multiplicity = 2(-1/2+1/2) +1 = 0+1 = 1
أو الحالة الثلاثية وتكون عندما يمتلك الالكترونيين مغزلية متشابهة
Spin multiplicity = 2(+1/2+1/2) +1 = 2+1 =3
في الحالة الخاملة ( قبل تسليط الضوء على المركب) يتواجد الإلكترونيين في الفلك HOMO والذي يكون π في المركبات الالكينية و n اللارابط في حالة مركبات مثل الكربونيلات. وعند تسليط طول موجي محدد ينتقل الإلكترون إلى الفلك LUMO والذي يكون بكلا الحالتين π* فيصبح هو الHOMO الجديد
وفقاً لقاعدة الإختيار Selection rules فعند إثارة الإلكترون و إنتقاله الى LUMO فأن المغزلية التعددية لا تتغير وبالتالي
الإنتقال من الحالة الاحادية الخاملة ( S0 ) إلى الحالة الأحادية المُثارة (S1) إنتقالة مسموحة بينما هي ممنوعة لـ S0 -> T1
أحياناً يتم إمتصاص طاقة أعلى من S1 وقد تصل إلى S3 أو S2 وهذه الحالات عادةً لا يتم فيها التفاعل فتنتقل إلى S1 معطيه طاقة على شكل حرارة تُسمى هذه العملية Internal conversions.
أن أغلب التفاعلات العضوية الضوئية تتم في T1 ( وهناك بعض الحالات تتم في S1) لذلك للمركب العضوي خياريين إما ينبعث الضوء ويرجع الإلكترون إلى الحالة الخاملة S1 -> S0 وهذه العملية تُسمى Fluorescence أو ينتقل الالكترون من S1 إلى T1 ( مستوى طاقة أقل بقليل من S1) وتُسمى هذه العملية Intercrossing system.
وفي هذه الحالة الالكترون لديه أيضاً خياريين آخرين إما الإنتقال من T1 إلى S0 رغم أنه إنتقال ممنوع إلا أنه يتم ببطء شديد ولذلك نصف عمره أطول ( معدل أقل ) من الانتقال من S1 إلى S0 و أقل شدة وتُسمى العملية Phosphorescence ولها طول موجي أعلى من Fluorescence بحكم أن فرق الطاقة فيها أقل.
أما الخيار الثاني هو حدوث تفاعل كيميائي من T1 وفي هذه الحالة يتكون عندنا ال Intermidate وتركيزه هو الذي يعتمد عليه معدل التفاعل الكيميائي وليس الحالة المثارة لأن ليس كل جزيء يُثار من الممكن أن يدخل في تكوين الناتج وهنا يكون لدينا ما يُسمى Quantum Yield (φ)وهو كمية الجزيئات المتفاعلة نسبةً إلى تلك التي تمت إثارتها
φ = عدد الجزيئات المتفاعلة عند زمن معين / عدد الفوتونات الممتصة عند نفس الزمن
وهذه القيمة عادةً تكون >١ ولكن قد تكون أعلى بسبب عدد الروابط المفككة عند تسليط الضوء.
بعض الحالات المركب العضوي قد يعطي نواتج مختلفة عندما يحدث التفاعل من S1 أو T1 .. اذا كان الناتج من S1 غير مرغوب أو الانتقالة لا تحدث من S1 إلى T1 بسبب فرق الطاقة الكبير فيمكن إضافة مركب يمتص الضوء عند طول موجي آخر فينقل طاقتها إلى T1 الخاص بالمتفاعل فتُسمى هذه العملية Photosensitization و المركب يُسمى Photosensitizer ... أحياناً هذا المركب يمتص الطاقة من T1 الخاصة بالمتفاعل إليه ويمنعه من التفاعل فتُسمى هذه العملية Quenching و المركب يُسمى Quencher.
وفي حالة ال Photosensitization فإن المركب Photosensitizer يمتص الضوء الى S1 ثم T1 .. حتى ينتقل إلى T1 الخاص بالمتفاعل فيجب أن تكون طاقة T1 الخاصة به أعلى بقليل T1 للمتفاعل و العكس صحيح مع ال Quenching حتى تمتص الطاقة من T1 في المتفاعل لابد تكون طاقته أعلى من طاقة T1 الخاص بال Quencher بقليل. هذه الحالتين هي حالات تندرج تحت Photo-physical process أي يجب أن لا تتفكك وتتفاعل مع نفسها أو وسط التفاعل أو مع المتفاعلات بل فقط تنقل الطاقة الممتصة أو تستقبلها. وهذا جدول يوضح بعض مركبات التي تندرج تحت الPhotosensitizers وأشهرها بنزوفينون و اسيتوفينون بسبب فرق الطاقة بين T1 و S1 منخفض و تمتص الضوء وتنقله بنسبة تصل الى ١٠٠%
مميزات الكيمياء الضوئية :
١- الحصول على نواتج بتراكيب كيميائية معقدة بخطوة واحده بدل القيام بعدة خطوات و بكميات كبيرة نسبياً
٢- تحقيق تفاعلات كيميائية ثيرموديناميكياً لا يمكن تتم بواسطة الحرارة
٣- تحقق نشاطية كيميائية لا يمكن الحصول عليها بدون الضوء و أحياناً لا يوجد محفزات لها
٤- الضوء يعتبر مصدر طاقة أرخص و أنظف وسهل الإستخدام
مساؤى الكيمياء الضوئية
١- بالغالب صعب التنبؤ بالنتائج وأحياناً خليط من النواتج ممكن الحصول عليه
٢- بعض المركبات لا يناسبها وسط التفاعل المحتوي على ضوء لأنها قد تؤدي الى تحللها ضوئياً
٣- بعض الحالات لا تكون الانتقائية الفراغية محققة أو نسبة الناتج منخفض
1 note
·
View note
Text
نسلط في هذا الجزء من المدونة الضوء على تفاعلي
Cycloaddition و Electrocyclic ring

وهذه التفاعلات مفسرة آلياتها و عملها بنظريتي
Hoffman-Wood rules و Frontier molecular orbital
وكلا النظريتيين حصلتا على جائزة نوبل بالتشارك ١٩٨٠... لكون هذه التفاعلات لا تعتمد على الميكانيكيات الأخرى بل تعتمدعلى حركة الالكترونات تستخدم هذه النظريتين الأوربتالات نوعها و تناظرها و طاقاتها و إمكانية تداخلها لتكوين روابط.

Frontier molecular orbital
اعتمد فيها اعالم Fukui على وضع أسس HOMO + LUMO دراستها تأثيرها على التفاعلات بالإضافة إلى طاقاتهم و العوامل المؤثرة عليها.
بينما Woodward & Hoffman اعتمدوا في دراساتهم على أشكال المدارات و خصائص الفصوص تداخلها و الـSymmetry الخاص فيها وطاقات هذه المدارات.
بعض المفاهيم التي وضعتها كلتا النظريتين لتسهيل فهم الدورالذي لعبته المدارات في تمكين التفاعل من عدمه بالإضافة إلى التنبؤ بالكيمياء الفراغية كون هذه التفاعلات تعتبر stereospecific.
HOMO : وهو أحد المدارات الجزيئية المحتوية على الكترونات ولكنه يتميز بأنه أعلاهم طاق��.
LUMO: وهو أحد المدارات الجزيئية الفارغة من الكترونات ولكنه يتميز بأنه أقلهم طاقة.
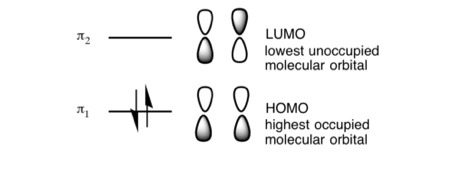
وهي تحدد كمية الطاقة اللازمة لإمكانية حدوث تفاعل وسهولة حدوث التفاعل
Suprafacial : وفيها يكون تداخل نفس المدارات الجزيئية لنفس الفصوص على نفس المستوى.
Antarafacial : وفيها يكون تدخل نفس المدارات الجزيئية لنفس الفصوص على مستوى مختلف.

conrotatory: تحصل في الجزيئات الناتجة من تفاعلات Electrocyclic حيث يقوم الجزيء بخطوة واحدة من فتح الحلقة أو إغلاق جزيء مفتوح. في حالة conrotatory يلتف المدارايين الجزيئيين المسؤوليين عن تكوين الرابطة الجديدة بنفس حالة الدوران مع أو ضد عقارب الساعة.
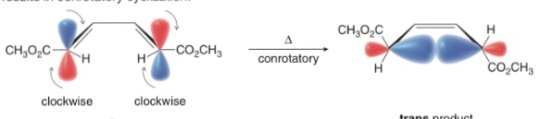
disrotatory: يلتف المدارايين الجزيئيين المسؤوليين عن تكوين الرابطة الجديدة بدوران متضاد حتى يتقابل الفصان القابلان للتداخل وتكوين رابطة
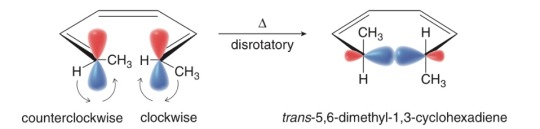
وتلعب هذه المفاهيم دوراً رئيسياً في شرح الحالة الفراغية للناتج والتنبؤ بها حيث أن أغلب تفاعلات percyclic لا تنتج ايزومرات لأنها regioselective.
ملاحظات/
١-تفاعلات Electrocyclic تفاعلات عكسية وعند العودة بالناتج الى المتفاعلات فقد تتغير فراغيتها.
٢- إستخدام ضوء أو حرارة قد يلعب دور في تغيير أو تحديد الكيمياء الفراغية للناتج.
١- الإضافة الحلقية Cycloaddition
يكون فيه متفاعلين لديهم القابلية على التفاعل مع بعضهم البعض مكونين حلقة تربطهم عن طريق تكسير روابط باي وتكوين روابط جديدة قد تكون سيجما و قد تكون باي مثلا تفاعل الشهير ديلز-الدر أو كما يُسمى نظامياً 2+4]] cycloaddition
وفي هذا التفاعل الدايين يتفاعل مع الكين لإنتاج حلقة ناتجة عن رابطتي سيجما + رابطة باي جديدة.
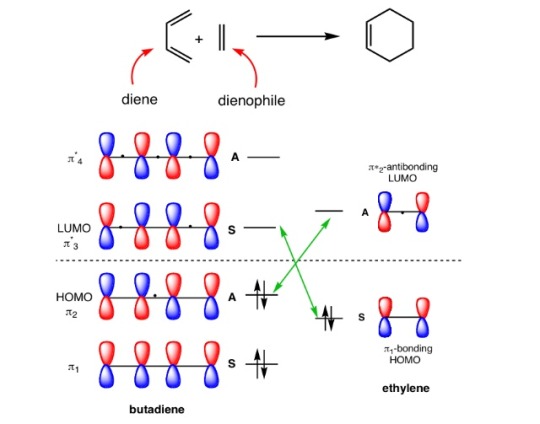
تفاعل ديلز الدر من مميزاته أنه ممكن يتكون حرارياً و ممكن يتكون ضوئياً لكن التفاعل بالضوء ينتج نسبة منخفضة لذلك الكثير يستخدم الحرارة لهذا التفاعل.
تفاعل ديلز-الدر ليس الوحيد بهذا النوع من التفاعلات فتفاعلات أخرى كثيرة أشهرها [2+2] cycloaddition يتم فيه تفاعل الكين مع الكين بدلاً من الدايين. هذا التفاعل لا يمكن يتم حرارياً ويتم فقط ضوئياً فوفقاً للنظريتين، فأن تفاعل[2+2] cycloaddition لا يتم بواسطة الحرارة لأن مدارات الـ HOMO و LUMO لا يمكن أن تتداخل بالإضافة إلى أن التفاعل لا يمكن أن يتم بواسطة Antarafacial لان الحلقة الناتجة صغيرة جداً وهذا قد يسببخلل فراغي وعدم إستقرار للناتج.
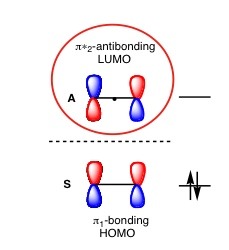
لذلك هناك حاجة مُلحة لوجود ضوء قادر يمتصه الالكترون فينتقل من HOMO الى LUMO فيصبح الـ LUMO عبارة عن HOMO جديد ولكن يمتلك دالة موجية مختلفة وإتجاه مداري مختلف يسمح له يتفاعل مع LUMO منجزيء آخر له نفس الدالة الموجية فتتكون حلقة رباعية مكونةمن رابطتي سيجما

وتفاعلات cycloaddition تتميز عن غيرها بأنها ممكن تكون Intermolecular و Intramolecular و أول تفاعل[2+2] cycloaddition كان من نوع intramolecular وبقي الباحثيين يستخدمونه لتحضير مركبات معقدة التركيب والتي لا يمكن تحضيرها بالطرق التقليدية حتى بداية الثمانينات تم اكتشاف بأن هذا التفاعل قد يخضع لـ intermolecular
2- Electrocyclic
وهو تفاعل بين جزيئي يكون ناتجه أما إقفال مركب لتكوينحلقة أو كسر رابطة سيجما لفتح حلقة.
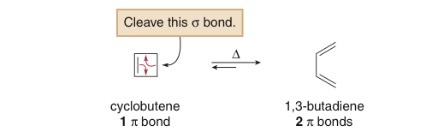

كما ذُكر سلفاً فأن تفاعلات Electrocyclic تعتمد على conrotatory و disrotatory فنوع الطاقة الخارجية المستخدمة ( حرارة أو طاقة) يلعب دور بهذا التفاعل فيعطي فراغية مختلفة.

حتى يتم توضيح مسألة لماذا التغيير بظروف التفاعل (حرارةأو ضوء) سيتم شرحها مثال مثال لإيضاح الفكرة:
عند تسليط ضوء على المدار الجزيئي الـ HOMO فإن الالكترون الموجود فيه سينتقل إلى الـ LUMO فيصبح هوالـHOMO الجديد. كمية الطاقة و الطول الموجي للضوءتعتمد على فرق الطاقة بين HOMO و LUMO قبل تسليط الضوء والتركيب الكيميائي في الجزيئي.
شكل المدار الجزيئي HOMO يحدده عدد روابط باي فيالجزيء. فإذا كان عددها زوجي فأن المدار p في طرف المركب سيكون معاكس للآخر وفالتالي فإن ناتج التفاعل فيوجود حرارة يكون trans.

بينما لو أُستبدلت الحرارة بضوء مع إبقاء عدد روابط باي كما هي فإن الالكترون سيقفز إلى HOMO جديد له دالة موجية مختلفة وكلا المداريين p بنفس الاتجاه فعندها سيسلك التفاعل سلوك disrotatory فينتج cis.

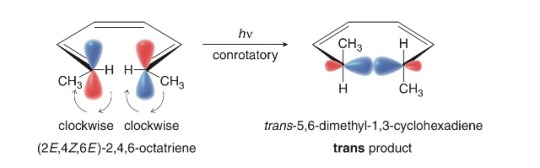
فإذا كان عددها فردي فأن المدار p في طرف المركب سيكون مشابه للآخر وفالتالي فإن ناتج التفاعل في وجود حرارة يكون cis .

بينما لو أُستبدلت الحرارة بضوء مع إبقاء عدد روابط باي كما هي فإن الالكترون سيقفز إلى HOMO جديد له دالة موجية مختلفة وكلا المداريين p عكس الاتجاه فعندها سيسلك التفاعل سلوك controtatory فينتج trans.

Sources:
http://ursula.chem.yale.edu/~chem220/chem220js/STUDYAIDS/pericyclic/PericyclicRxn.pdf
https://www.asu.edu/courses/chm332/PericyclicReactions.pdf
https://ocw.mit.edu/courses/chemistry/5-13-organic-chemistry-ii-fall-2006/lecture-notes/lec_15_16_17_06.pdf
https://dasher.wustl.edu/chem430/lectures/lecture-21.pdf
0 notes
Text
Controlled radical polymerization (Brief introduction).
مقدمة
تندرج المواد البوليمرية تحت مركبات كيميائية تُسمى “
Macromolecules
" أي الجزيئات الضخمة أوالعملاقة إلا أن البوليمرات تتميز عن بقايا الجزيئات المُدرجة تحت هذا التصنيف بأنها مكونة من جزيئات صغيرة متراصة و مترابطة بروابط تساهمية تُسمى"مونمر". التركيب الكيميائي للمونمرات يسمح لتدرج التحضيرات البوليمرية إلى صنفين:
البلمرة بالتكاثف أو البلمرة الخطية “Step growth"
يتميز التركيب الكيميائي للمونمرات المصنفة ضمن هذا النوع بأنها قادرة على التفاعل مع بعضها البعض لينتج البوليمر كناتج رئيسي و نزع جزيء صغيركالماء. ومثال على هذا الصنف هو تفاعل الأحماضالأمينية مع بعضها البعض وبنزع جزيء الماء من طرفي الحمض الأميني و تحضير نايلون ٦,١٠ أو٦,٦. وفي هذا النوع لا يحصل تدخل من قبل أيونات موجبة وسالبة ولا كذلك جذور حرة.

البلمرة بالإضافة "Chain growth"
ويلزم في التركيب الكيميائي لمونمرات أن تحتوي على رابطة مضاعفة. وجود الكترونات باي يجعلها أكثرعُرضة للهجوم من قبل الجذر الحر حيث يكون الالكترون الوحيد بالجذر رابطة سيجما قوية مع أحدى الكتروني الرابطة المضاعفة فينتج عن ذلك جذر جديد يهاجم رابطة مضاعفة في مونمر آخر و هكذا تستمرالبلمرة.

خطوات ميكانيكية البلمرة بالجذر الحر
البدء "Initiation" .1
تُعتبر هذه الخطوة هي الخطوة الأسرع من بين الخطوات الثلاث وفيها تقوم البادئة "Initiator" بإنتاج جذور حرة بطرق مختلفة تختلف بأختلاف التركيب الكيميائي للبادئة أما بتسخين المحلول أو تسليطه بأشعةUV أو بإضافة حفاز. من المعروف بأن الجذور الحرة ذات نشاطية عالية لذلك بمجرد إنتاجها تبدأ الهجوم على المونمرات بعد الهجوم على المونمر يُصبح الناتج جذر جديداً جزيء أكبر يهجم على مونمر آخر وهكذا.

النمو "Propagation" .2
عندما يهجم الجذر على جزيء أو اثنين من المونمر يبقى الناتج جذراً نشطاً مالم يتم تثبيط بعامل معين. هذا الجذر يستمر بالنمو عن طريق إضافة مونمر إلى سلسلته وتُسمى هذه العملية بالنمو. تختلف سرعة عملية النمو بإختلاف نوع المونمر لذلك كل مونمر يمتلك ثابت يُسمى ثابت النمو ورمزه Kp. ويُعبر هذا الثابت بأنه عدد الوحدات التي تُضاف للسلسلة النشطة في الثانية.

الإنهاء "Termination" .3
بشكل عام هذه الخطوة تؤدي إلى توقف السلسلة البوليمرية النشطة على التمدد و إضافة وحدات مونمرية أخرى للسلسلة. لسوء الحظ هذه العملية قد تتم بأي لحظة من لحظات البلمرة ولها طُرق مختلفة أبرزها:
الإندماج "Combination"
وبهذه الطريقة يلتقي جذريين من سلسلتيين نشطة ويرتبطان مع بعضهما البعض برابطة أحادية. قد تكون السلسلتين لهما نفس الطول أو أحدهما أقصر. ربما يكون أحد الجذريين سلسلة بوليمر و الآخر ليس كذلك.

الإنتقال لمونمر أو مذيب
وفيه يقوم جذر السلسلة النشطة بنقل الجذر إلى جزيء مونمر أو مذيب كنزع هيدروجين بكسر الرابطة الأحادية للهيدروجين بالمونمر أو المذيب والنتيجة تكون سلسلة بوليمرية مثبطة و جذر جديد يقوم بمهاجمة مونمرات أخرى.

Disproportionation
قد تتواجد سلسلتي بوليمر نشطة إلا أن الجذريين الحريين عوضاً عن الإرتباط مع بعضهما البعض كما في تفاعل الإندماج فأن أحد الجذريين يقوم بنزع هيدروجين من ذرة الكربون المجاورة مباشرةً للجذر فينتج عن ذلك سلسلتين مُثبطة أحدهما تحتوي على ميثايل بالنهاية و الأخرى يتفاعل جذريها المجاوريين مكونان رابطة مضاعفة.

نزع هيدروجين من منتصف بوليمر آخر H-Abstraction
قد تقوم سلسلة نشطة بنزع هيدروجين من منتصف سلسلة بوليمر نشط آخر فتُصبح مثبطة وغير قابلة للنمو أكثر بينما سلسلة البوليمر الأخرى يُصبح لديها جذر جديد غير الجذر الطرفي فإما يستمر كلا الجذريين بالنمو أو في حال كانت المسافة بينهما كافية يُصبح تحلق و يتكون سلسلة حلقية.
خطوة الإنهاء تمتلك ثابت يُسمى ثابت الإنهاء Kt وهويعتمد على تركيز الجذر الموجود في جميع الطرق لإنهائية التي تمت مناقشتها سابقاً لذلك بوجود هذه الطرق تُصبح إحتمالية تثبيط و قتل السلاسل البوليمرية واردة بشكل أكبر خصوصاً بالثلث الأخير من زمن البلمرة بسبب التنافسية بين Kp و Kt.

عيوب البلمرة بالجذر الحر
لذلك فأن البلمرة بالجذر الحر تؤدي إلى سلاسل ذات أطوال مختلفة في المحلول الواحد. كذلك يصعب التحكم بتركيب السلسلة البوليمرية بسبب نشاط الجذرالعالي و خروجه عن السيطرة. كذلك يصعب بالغالب التأكد من تواجد المجاميع الناشئة من تفكك البادئة في بداية أو نهاية السلسلة البوليمرية وإن وُجدت فلن تكون بجميع السلاسل البوليمرية. هذه المجاميع قد تكون مهمة في تطبيقات معينة. على سبيل المثال قد تحتوي على مجاميع نشطة ضوئياً تسمح بتتبعها أو مجاميع منالممكن أن تتفاعل إختيارياً مع مجاميع معينة في مواد حيوية هالجسر الكبريتي أو مجاميع الأمين في الحمض الأميني لايسين أو بالكحولات في السكريات أو مجاميع تسمح بربط بوليمر A ببوليمر B دون الخوض في تفاعلات الجذور. وجود عينة بوليمر تحتوي على سلاسل بوليمر بمدى أطوال كبير يجعلها غير مناسبة للتطبيقات الطبية الحيوية لأن كل مدى داخل هذا المدى الواسع له خصائص مختلفة.
ويتضح من ذلك بأن البوليمرات المُحضرة بالجذرالحر قد لا تتناسب مع العديد من التطبيقات بينما لابأس بها في تطبيقات صناعية معينة. كذلك تحِد منتحضير بوليمرات بتراكيب مختلفة قد يكون لها تطبيقات جديدة أو تساهم بشكل أفضل.
البلمرة الحية "Living polymerization"
قبل عام ١٩٥٦ لم يكون هنا سوى بلمرة بالجذر الحر وكان يُعتقد بأن التحكم بالجذور الحرة أمر ميؤس منه ويجب تقبل هذه الحقيقة حتى قام العالم Szwarc بتحضير بولي ستايرين بواسطة البلمرة الأنيوية.تختلف البلمرة الأنيونية عن البلمرة بالجذر الحر ليس فقط بنوع البادئة و أن الذي يهاجم الرابطة المضاعفة وينمي السلسلة البوليمرية هو الشحنة السالبة بدل الجذرالحر بل كذلك لا تتواجد أي عملية من عمليات الإنهاء السابق ذكرها و بالتالي فأن السلاسل البوليمرية تنمومعاً و بنفس الطول تقريباً ولذلك قيمة PDI تقترب إلى١ بدل من إن تكون عالية مثل البلمرة بالجذر الحر.
( ملاحظة قيمة PDI هي ناتج قسمة Mw على Mn وكلما إقتربت من الواحد يعني بأن جميع السلاسل لها نفس الوزن الجزيئي و أطول. في الجزيئات الصغيرة لأن أوزانها الجزيئية واحدة تكون PDI لهم تساوي ١دائماً).

أُعتبرت هذه الطريقة ثورة في مجال البوليمر وتمتحضير العديد من البولميرات بالبلمرة الكاتيونية والأنيونية لمونمرات كانت تتبلمرة بالجذر الحر ودراسة إختلاف خصائصها عند بلمرتها بالجذر الحر وبالبلمرة الحية.
لذلك كان التساؤل كيف يتم تطبيق مفهوم living polymerization على الجذور بدل الشحنات ؟ لأن الشحنات المتشابهة تتنافر وليست بنشاطية الجذرالعالية لذلك عملية الإنهاء إحتماليتها قليلة خلال البلمرة والسلاسل متساوية تقريباً. ومن هذا التساؤل ظهر مايُسمى بـ البلمرة الحية "المتحكمة" للجذر (Controlled “living” radical polymerization).
البلمرة الحية للجذر " Living radical polymerization "
العامل المهم في البلمرة الحية هو التقليل قدر الإمكان من تركيز الجذر الحر. فكما ذُكر سابقاً بأن عملية الإنهاء تعتمد على تركيز الجذر الحر وإلا فأن السلاسل البوليمرية ستتعرض للتثبيط و التوقف عن التمدد.والهدف في البلمرة الحية للجذر هو ألا تتوقف السلاسل البوليمرية بالنمو. لذلك يتم إيقاف بعض السلاسل النشطة مؤقتاً و ترك البعض الآخر ينمو والعملية بينتوقف نشاط الجذر مؤقتاً و تنشيطه عملية عكسية هدفها التقليل من تركيز الجذور الحر.
هناك طرق كيميائية عديدة يُستخدم فيها البلمرة عن طريق التحكم بالجذور الحرة للحصول على بوليمرات لها خصائص مشابهة لتلك المُحضرة بالبلمرة الكاتيونية أو الأنيونية. من أوائل و أشهر تلك الطرق إستخداماً :
Nitroxide mediated polymerization(NMP)
هذه الطريقة يُستخدم فيها جذر NO• يقوم هذا الجذربالتفاعل مع جذر بوليمري نشط فيثبطه ثم عند زياد ةدرجة الحرارة تنكسر الرابطة معطية جذر NO• وسلسلة بوليمرية نشطة جذرياً تستمر بمهاجمة المونمرات النمو. هذه الطريقة تسمح بالتحكم بالجذرالحر لكن من عيوبها إستهلاك طاقة حرارية.

Reversible addition-fragmentation chain transfer (RAFT)
عامل RAFT هو جزيء يحتوي على مجموعة وظيفية تُسمى thiocarbonylthio يحتوي هذا العامل على ذرتي كبريت أحداهما مكونة رابطة مضاعفة مع ذرة كربون مرتبطة بعامل ثابت Z والأخرى مرتبطة بنفس الكربون برابطة أحاديةومرتبطة بمجموعة R. تقوم سلسلة بوليمرية نشطة بالهجوم على الرابطة S=C مكونة جذر على ذرة الكربون التي تقوم بكسر الرابطة من ذرة الكبريت الأخرى مكونة رابطة مضاعفة على الجهة المقابلة وجذر نشط يهاجم المونمرات لتكوين سلسلة بوليمرية وهكذا. عند الهجوم على هذا العامل فأن الجذرالكربوني و الرنين الحاصل تختلف ثباتيته بإختلاف المجموعة Z لذلك تختلف هذه المجموعة بإختلاف نوع المونمر و المذيب المُستخدمين.

Atom transfer radical polymerization(ATRP)
تُعتبر طريقة ATRP مُستوحاة من تفاعل atom transfer radical addition (ATRA) وفيها تتم إضافة هاليد الألكيل إلى مجموعة الكين مكونة ناتج هاليد الكيل ذو وزن جزيئي أكبر من الهاليد الالكيل المتفاعل.
في طريقة ATRP يتم إستخدام هاليد الألكيل كبادئة وبهذه الطريقة يجب إستهلاك البادئة كلياً بالبداية وإلا فأن الوزن الجزيئي يُصبح أكبر من النظري. يتم تنشيط البادئة و إنتاج جذر منها عن طريق حفاز معدن. من مزايا المعدن الحفاز أن يسهل عليه التحول من حالة أكسدة n إلى حالة أكسدة بعد نزع الهاليد أخرى n+1وبذلك يدخل هذا المعدن بحالتي الأكسدة في تفاعل عكسي مع سلسلة البوليمر النشطة بالجذر و نظيرها المثبط بالهاليد القادم من المعدن بحالة الأكسدة العالية.في الغالب يتم إستخدام النحاس Cu كحفاز بسبب وفرته العالية و رخصه مقارنة بمعادن أخرى كالروثينيوم. و يُعتبر مُفضل مقارنة بالنحاس لأنه أعلى نشاطاً منه. في ميكانيكية ATRP يكون النحاس ذوالأكسدة المُنخفضة CuX
هو المنشط ودوره هو نزع الهاليد من الكربون نزعاً متساوياً بحيث ينتج جذر ألكيلي نشط يُهاجم الرابطة المضاعفة بالمونمر و يكون سلسلة نشطة و معدن بحالة الأكسدة العالية CuX2. ثم يتم تثبيط الجذرالنشط بالمعدن ذو الأكسدة العالية CuX2 وهو المثبطب واسطة الهاليد ليتكون CuX و P-X. في هذه العملية العكسية يوجد ثابتين وهما ثابت التنشيط Kact و ثابت التثبيط Kdeact وللحصول على بلمرة حية مُتحكمة لابد يكون Kdeact > Kact لتقليل تركيز الجذر النشط و تجنب عملية الإنهاء. وبهذه الطريقة كلما زادت نسبة تحويل المونمر تقل قيمة PDI وهي المطلوبة لتكون البلمرة حية و متحكمة "Controlled".

يتم معرفة البلمرة إذا كانت حية أو جذر حر حركياً عن طريق رسم منحنى ln(M0/M) مقابل الزمن فتكون العلاقة خطية إذا كانت البلمرة تفاعل من الدرجة الأولى معتمداً على تركيز المونمر أما إذا المعدل يعتمد على تركيز الجذر أيضاً فأن البلمرة تكون غير مُسيطرة و تصبح جذر حر. أحياناً يحصل إنحراف طفيف في العلاقة يكون سببه كفاءة البادئة نفسها لأنها لا تُستهلك بشكل كلي بسرعة في البداية.

هذه الطرق مكنت المتخصصين بالبوليمر من تحضيربوليمرات بأشكال هندسية مختلفة و تكوين بوليمرات بتراكيب محددة و مختلفة. بالإضافة إلى الحصول على مجاميع بنهاية و بداية السلسلة تكون مطلوبة لتطبيقات معينة أو من الممكن تعديلها للحصول على مجاميع أخرى تُساعد في توظيف السلسلة البوليمرية بطرقأخرى. على سبيل المثال، بطريقة ATRP يتم الحصول على هالوجين بآخر السلسلة يمكن إستبداله بمجموعة أزيد و ربط البوليمر بجسيمات نانوية تمتلك مجموعات الكاين على سطحها بواسطة Click reaction.

REFERNCE
https://pubs.acs.org/doi/abs/10.1021/acs.chemrev.5b00671
https://www.sciencedirect.com/science/article/pii/S0079670007000044
https://www.cmu.edu/maty/chem/fundamentals-atrp/index.html
2 notes
·
View notes
