#cellules contractiles non musculaires
Photo
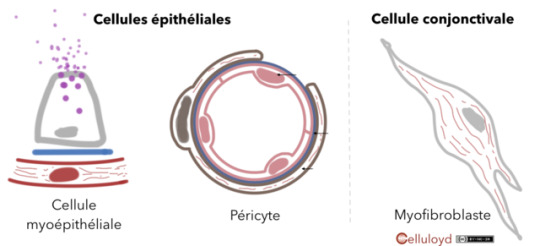
Cellules contractiles non musculaires
Il existe un certain nombre de cellules qui ne sont pas musculaires, et qui pourtant sont capables de contraction. Citons les cellules myoépithéliales (phénotype épithélial et conjonctival) dans les épithéliums glandulaires servant à « presser » les portions sécrétrices des glandes pour excréter plus rapidement leurs substances, les péricytes (phénotype épithélial et conjonctival) autours des capillaires sanguins pour réguler finement la micro-circulation, ou les myofibroblastes (phénotype épithélial) qu'on trouve dans les tissus conjonctifs en cours de cicatrisation.
Ces schémas ont été faits pour mes ED du Tutorat à partir des cours que j'ai retranscrit quand j'étais en première année de médecine. Ma seule source est le professeur de l'époque, et je peux avoir mal compris certaines choses, faire des approximations fausses, etc même si je fais de mon mieux. Croiser les sources permet d'avoir des informations plus fiables. N'hésitez pas à commenter pour discuter des sujets abordés ! Schémas et explications faits entre 2015 et 2016.
#histologie#tissus musculaires#cellules contractiles non musculaires#medecine#paces#ue 2#biologie#science#corps humain#studyblr#medblr#scientific illustration
1 note
·
View note
Photo

MYTHE EN MUSCULATION ( LA GRAISSE SE TRANSFORME EN MUSCLE )
Peut-être que cette affirmation te paraît ridicule, pourtant, beaucoup de personnes croient encore que le muscle et la graisse ne font qu’un. Selon ces personnes, il suffirait de commencer la musculation pour “transformer” sa graisse en muscles.
Ils affirment également qu’une grande masse musculaire vieillit très mal dans le temps, au point de se transformer en graisse. Quelle grosse blague...
Et après, ils prétendent que c’est pour cette raison qu’ils ne font pas de musculation.
Pour commencer, chaque cellule de ton corps dispose de ce que l’on appelle une membrane plasmique. Cette membrane est composée essentiellement de lipides. (graisse)
Tu trouves donc de la graisse sous ta peau, entre tes muscles ou encore, entre tes organes vitaux. (plus communément appelée, graisse viscérale)
Tu l’auras compris, la graisse souvent diabolisée fait partie intégrante de ton corps, que tu le veuilles, ou non.
Pour en revenir au sujet principal, les muscles sont, quant à eux, des tissus contractiles, ayant un point d’insertion et un point de terminaison. Par exemple, le grand pectoral s’insère sur la clavicule ainsi que le long du sternum et se termine sur l’humérus.
Comme dit précédemment, le muscle est un tissu contractile. Il est composé de filaments fins d’actine et de filaments épais de myosine, qui interagissent entre eux pour raccourcir le muscle et provoquer sa contraction.
En lisant ça, tu peux facilement en conclure que la graisse et le muscle sont 2 tissus complètement différents. Si l’on reprend l'hypothèse selon laquelle, “la graisse se transforme en muscle, cela n’a tout bonnement aucun sens.
0 notes
Text
Le diabète de type 2 sur la voie de la rémission
Réveiller les cellules du pancréas productrices d’insuline grâce à un régime strict ou en faisant travailler certains muscles : ces deux nouvelles approches viennent de démontrer leur efficacité pour soigner enfin cette affection chronique.
Personne n'aurait osé l'espérer il y a encore dix ans. Pourtant, maintenir dans le temps, sans injections d’insuline ni aucun autre traitement, une bonne régulation de la glycémie chez les patients atteints de diabète est aujourd’hui un objectif atteignable. Autrement dit, "faire entrer le diabète de type 2 en rémission" et "retourner à un état non diabétique, sans médicaments antidiabétiques ou antihypertenseurs", selon l’essai clinique mené par le Pr Roy Taylor et son équipe de l’université de Newcastle (Royaume-Uni) dont les conclusions ont été publiées dans la prestigieuse revue The Lancet en juillet dernier. Des résultats qui changent la donne dans le traitement de cette maladie chronique qui touche au moins 3,5 millions de personnes en France. 150 participants diagnostiqués depuis moins de six ans ont ainsi été soumis au "protocole de Newcastle", un traitement de choc consistant à perdre 15 kg en trois à cinq mois, grâce à un régime limité à environ 840 kcal/jour. Soit presque trois fois moins que l’apport calorique "normal". Un an après leur retour à un régime alimentaire équilibré, 90 % de ceux qui avaient réussi à perdre 15 kg étaient en rémission, et 50 % pour l’ensemble : leur glycémie était à nouveau autorégulée, sans aucun traitement.
Des cellules en hibernation à nouveau stimulées
Le mécanisme en jeu a été percé à jour par les spécialistes. Plus efficace que le régime strict habituellement suivi par les malades, le protocole de Newcastle - très peu calorique - déclenche en fait des signaux d’alerte dans l’organisme pour stimuler des cellules particulières situées dans le pancréas (cellules bêta), sécrétant l’insuline. Or, en raison de facteurs d’hérédité ou d’une alimentation trop riche, ces cellules ne sont normalement plus en mesure de produire cette hormone dans le pancréas des diabétiques de type 2 car elles sont épuisées, voire détruites. "Mais Roy Taylor a découvert que nombre de cellules bêta qu’on pensait mortes ne l’étaient pas ! Elles étaient en fait comme en hibernation", explique le Dr Karim Bouzakri, directeur de recherche au Centre européen d’étude du diabète (CEED), à Strasbourg. Résultat : les signaux de détresse provoqués dans l’organisme par la période de carence profonde finissent par les réveiller. "Ils indiquent en effet au pancréas que l’organisme n’est plus en situation hyperglucidique et calorique : ces cellules, jusqu’alors en dormance, peuvent à nouveau fournir de l’insuline." Selon les données de l’étude, plus le diabète est récent plus le patient a de chances de répondre positivement. "Le message est clair : cette nouvelle approche par la perte de poids devrait être conseillée pour tous les patients, en particulier au moment du diagnostic", affirme Roy Taylor.
La myokine X, molécule prometteuse
"En affirmant que l’on pouvait obtenir une rémission du diabète de type 2, Roy Taylor a voulu donner un coup de pied dans la fourmilière pour faire bouger les choses. Mais il y a effectivement une vraie volonté dans la recherche de trouver d’autres voies de traitement", analyse Karim Bouzakri. En particulier en utilisant des moyens détournés pour forcer l’organisme à inverser, ou au moins mieux gérer, la maladie. Au CEED, l’équipe du chercheur creuse une piste tout aussi innovante : exploiter la capacité de certaines molécules, sécrétées par le muscle et libérées dans le sang (myokines), à venir en renfort du pancréas."Plus qu’un simple organe contractile, le muscle fonctionne presque comme une glande endocrine à part entière", explique Karim Bouzakri. Chaque muscle sécrétant des myokines différentes, l’un d’entre eux s’est révélé particulièrement bénéfique comme l’a révélé la dernière découverte de l’équipe publiée en juillet dernier dans Scientific Report : le triceps (muscle de la face postérieure du bras). Même si l’influence d’autres muscles ne peut être négligée. "Nous travaillons sur des muscles cultivés in vitro à partir d’échantillons prélevés sur des patients ou des personnes saines, détaille Karim Bouzakri. Ils conservent leur signature génétique et reflètent donc parfaitement ce qui se passe in vivo au niveau moléculaire." Et le triceps présente deux avantages : "Il dispose de davantage de fibres consommant du glucose, et il ne devient pas insulino-résistant." Autrement dit, il conserve donc toutes ses capacités d’absorption du sucre dans le sang.
En échange de quoi, il relâche ses myokines dans l’organisme, celles-ci boostant les cellules bêta du pancréas et améliorant ainsi son activité. "C’est une communication croisée qui s’instaure entre muscle et pancréas, un véritable dialogue", s’enthousiasme celui qui fait figure de pionnier dans ce domaine. L’équipe a ainsi identifié une molécule en particulier. « Nous l’appelons encore la “myokine X” car notre brevet est en cours d’examen", précise Karim Bouzakri. Outre son action bénéfique sur le pancréas, celle-ci présenterait un grand intérêt pour un certain profil de patients diabétiques de type 1 : ceux candidats à une greffe - au niveau du foie - des îlots de Langerhans, ces ensembles de cellules du pancréas qui abritent les cellules bêta sécrétrices d’insuline. "Lors de cette opération, 70 % des îlots se perdent en raison de l’inflammation provoquée lors de leur injection et du manque de vascularisation du foie. Or un traitement de ces îlots avec notre “myokine X” induit une protection contre ces effets délétères", explique le chercheur. L’objectif principal des scientifiques reste cependant d’utiliser cette molécule pour conduire chaque cellule bêta à produire elle-même davantage d’insuline de façon autonome. "Notre but, c’est vraiment de pouvoir “inverser” la maladie", insiste-t-il, afin de stopper la dégradation du pancréas. De sorte que les patients puissent éviter les traitements de long terme, en se nourrissant de façon équilibrée, sans mesures privatives.
Faire des haltères est plus efficace que de marcher
Autre intérêt des recherches en cours : confirmer le type d’exercices physiques à préconiser aux patients, bien loin du jogging quotidien habituellement prescrit. "Il faut faire des haltères, même assis", lance Karim Bouzakri. En effet, contrairement aux exercices d’endurance, ceux de résistance musculaire permettent la sécrétion des myokines protectrices car ils sollicitent "des muscles ayant une forte proportion en fibres glycolytiques, comme le triceps". Ce type d’activité permet de mieux absorber le glucose sanguin et donc de mieux réguler la glycémie. "Aujourd’hui encore, on préconise de faire vingt minutes de marche par jour alors que des exercices de musculation seraient bien plus pertinents ! Car les mouvements de résistance permettent non seulement au muscle d’aller pomper le sucre dans le sang, mais aussi de créer plus de masse musculaire, et donc davantage de fibres sécrétrices de myokines", explique le spécialiste.
Pis, l’endurance pourrait avoir des effets néfastes chez les diabétiques obèses. "L’endurance tend à rajouter de l’inflammation dans une situation déjà inflammatoire. C’est un phénomène que nous avons bien montré lorsque je travaillais au Centre d’inflammation musculaire de l’Institut Karolinska en Suède." En outre, alors que la consommation de glucose par les muscles se limite au temps de l’activité pratiquée dans le cas de l’endurance, les fibres activées durant les exercices de résistance continuent de pomper le sucre bien après les séances. Pour l’heure, la myokine X est encore au stade préclinique, les essais n’ayant pas encore été menés sur l’humain. "Il y a encore des détails à régler : faut-il amener le muscle à produire plus de myokines ou, au contraire, apporter directement ces molécules dans la circulation sanguine par le biais d’un traitement, et dans quelle proportion ?", s’interroge Karim Bouzakri.
"Redémarrer " le métabolisme de l’intestin
Mais 2018 aura aussi vu une autre stratégie non moins "spectaculaire" pour tenter de vaincre le diabète selon les auteurs d’une étude internationale publiée dans la revue Gastrointestinal Endoscopy et conduite auprès de 50 patients. Il s’agit cette fois de brûler la muqueuse du duodénum, la partie de l’intestin grêle située juste après l’estomac. L’opération se déroule sous anesthésie légère et consiste à introduire un cathéter par la bouche jusqu’à cette portion du système digestif qui joue un rôle majeur dans l’assimilation des sucres et la régulation de la glycémie. Là, un ballon est gonflé avec une eau chauffée à 86 °C afin de brûler les cellules et bactéries de surface sur un tronçon d’une quinzaine de centimètres. L’idée étant d’opérer une sorte de "redémarrage" du métabolisme de l’intestin. "Les anomalies de la muqueuse du duodénum, qu’elles concernent la capacité à absorber les nutriments ou les cellules entéroendocrines [ayant un rôle hormonal dans l’intestin] interviennent dans le développement de la résistance à l’insuline chez les diabétiques de type 2", écrivent les auteurs de l’expérience. Ainsi, en détruisant cette muqueuse défaillante, l’intervention permet à de nouvelles cellules "naïves" de venir retapisser l’intestin. Un "resurfaçage muqueux du duodénum" qui s’est révélé très efficace chez l’ensemble des patients inclus dans l’essai. Même un an après l’intervention, le diabète était stabilisé chez 90 % d’entre eux. "Nous avons vu une amélioration spectaculaire de la glycémie dès le lendemain de l’opération, avant même que les patients ne perdent un seul kilo", détaille Jacques Bergman, auteur de l’étude et professeur de gastroentérologie au Centre médico-universitaire d’Amsterdam (Pays-Bas). Autant de traitements qui laissent augurer que la guérison du diabète n’a sans doute jamais été aussi proche.
Une maladie de plus en plus présente chez l’enfant
C’est une nouvelle maladie en pédiatrie. Le diabète de type 2, longtemps surnommé « diabète adulte » en raison de son apparition tardive, est de plus en plus courant chez les enfants et les adolescents. Dans certains pays comme le Japon, il devient même plus fréquent que le type 1 qui se déclare, lui, classiquement chez le sujet jeune. Une progression constante est ainsi observée depuis plusieurs années à la faveur de l’épidémie mondiale d’obésité. Une augmentation particulièrement préoccupante chez certains groupes ethniques à risque (Afro-américains, Amérindiens, Asiatiques). En France, 8 % des enfants diabétiques seraient atteints du type 2. Soit quatre fois plus qu’il y a dix ans. Un phénomène qui alerte d’autant plus que l’apparition de complications chez ces jeunes patients serait à la fois plus précoce et plus rapide.
Le diabète désormais classé en 5 formes
Insulino-dépendant sévère (type 1) Il concerne des malades avec un indice de masse corporelle faible, un déficit d’insuline et des anticorps témoignant d’une origine auto-immune de la maladie.
Insulino-déficient sévère Les malades souffrent d’un déficit de production d’insuline proche du type 1, mais leur système immunitaire n’est pas impliqué. Le risque de rétinopathie est plus important.
Insulino-résistant sévère Il touche des patients en surpoids ou obèses chez qui les cellules ont développé une résistance à l’insuline rendant l’absorption du glucose plus difficile. Il accroît les risques d’atteinte rénale et hépatique.
Insulino-résistant léger Les malades en surpoids ou obèses ont un mode de vie à l’origine d’une dérégulation de la glycémie mais avec une résistance à l’insuline faible.
Insulino-sénescent Il recouvre des diabètes légers liés à l’âge. Il proviendrait essentiellement d’un vieillissement du pancréas.
0 notes
Photo

Léiomyocytes spéciaux
Les léiomyocytes sont des cellules musculaires dont les protéines contractiles ne sont pas organisées sous forme de myofibrilles, ce qui leurs donnent au microscope optique un aspect non strié mais lisse : c'est pourquoi on parle aussi de cellules musculaires lisses. Ils sont principalement voués à la mobilité involontaire des viscères, mais il existe certains léiomyocytes dont la fonction n'est pas uniquement de se contracter.
Les cellules de Ruyters sont des léiomyocytes possédant une fonction endocrine, en sécrétant de la rénine dans le sang, une hormone adressée au rein. Les cellules rameuses sont des léiomyocytes de la média des gros et moyens vaisseaux, capables de synthétiser leur matrice extra-cellulaire composée entre autre de fibres élastiques. Enfin les cellules de Cajal sont capables de se dépolariser spontanément comme un pacemaker pour initier une onde de contraction aux autres léiomyocytes avec lesquels elles sont liées (on parle de muscle lisse unitaire).
Ces schémas ont été faits pour mes ED du Tutorat à partir des cours que j'ai retranscrit quand j'étais en première année de médecine. Ma seule source est le professeur de l'époque, et je peux avoir mal compris certaines choses, faire des approximations fausses, etc même si je fais de mon mieux. Croiser les sources permet d'avoir des informations plus fiables. N'hésitez pas à commenter pour discuter des sujets abordés ! Schémas et explications faits entre 2015 et 2016.
#histologie#tissus musculaires#leiomyocytes speciaux#medecine#paces#ue 2?biologie#science#corps humain#studyblr#medblr#scientific illustration
3 notes
·
View notes
Photo

Muscle lisse unitaire
Les léiomyocytes sont des cellules musculaires dont les protéines contractiles ne sont pas organisées sous forme de myofibrilles, ce qui leurs donnent au microscope optique un aspect non strié mais lisse : c'est pourquoi on parle aussi de cellules musculaires lisses. Ils peuvent être regroupés dans les tissus de façon unitaire ou multi-unitaire selon les relations entre les cellules.
Dans les muscles lisses unitaires, la lame basale (un isolant électrique) est discontinue entre les cellules, et ces dernières sont reliées par des jonctions communicantes (ou gap junctions) qui permet la libre circulation de ions et donc des dépolarisation membranaire d'une cellule à l'autre ce qui permet une synchronisation électrique de ces cellules, et donc des contractions. La dépolarisation se déplace de proche en proche dans les cellules ce qui créé une onde de contraction, qu'on appelle péristaltisme lorsque cela concerne un conduit (comme le péristaltisme digestif). Les muscles lisses unitaires sont des structures qu'on retrouve à certains muscles lisses comme ceux qui se trouvent sous les muqueuses (appareil digestif, urinaire et génital).
Ces schémas ont été faits pour mes ED du Tutorat à partir des cours que j'ai retranscrit quand j'étais en première année de médecine. Ma seule source est le professeur de l'époque, et je peux avoir mal compris certaines choses, faire des approximations fausses, etc même si je fais de mon mieux. Croiser les sources permet d'avoir des informations plus fiables. N'hésitez pas à commenter pour discuter des sujets abordés ! Schémas et explications faits entre 2015 et 2016.
#histologie#tissus musculaires#muscle unitaire lisse#medecine#paces#ue 2#biologie#science#corps humain#studyblr#medblr#scientific illustration
3 notes
·
View notes
Photo

Protéines du cytoplasme des léiomyocytes
Les léiomyocytes sont des cellules musculaires dont les protéines contractiles ne sont pas organisées sous forme de myofibrilles, ce qui leurs donnent au microscope optique un aspect non strié mais lisse : c'est pourquoi on parle aussi de cellules musculaires lisses.
Leurs cytosquelette est un réseau extensif de protéines fibrillaires dans le cytoplasme en trois dimensions ancrées sur la membrane : ainsi lorsque les protéines motrices en raccourcissent les fibres, toute la cellule se rétracte sur elle même. Les jonctions membranaires sont de deux types : les plaques d'adhérences fixent les filaments intermédiaires de desmine, et les zonula adherens fixent ls filaments d'actines des myofilaments fins.
Les zones denses sont des jonctions intra-cytoplasmiques entre filaments intermédiaires et actine fibrillaire. Elles contiennent des myofilaments épais, qui sont moins nombreux que chez les cellules musculaires striées : pour un myofilament épais de léiomyocyte sont associés plus de myofilaments fins que dans les myofibrilles. Les myofilaments fins gardent à peu près la même structure que dans les cellules musculaires striées, sauf que la troponine est remplacée par la caldesmone et la calmoduline.
Ces schémas ont été faits pour mes ED du Tutorat à partir des cours que j'ai retranscrit quand j'étais en première année de médecine. Ma seule source est le professeur de l'époque, et je peux avoir mal compris certaines choses, faire des approximations fausses, etc même si je fais de mon mieux. Croiser les sources permet d'avoir des informations plus fiables. N'hésitez pas à commenter pour discuter des sujets abordés ! Schémas et explications faits entre 2015 et 2016.
#histologie#tissus musculaires#proteines du cytoplasme des leiomyocytes#medecine#paces#ue 2#biologie#science#corps humain#studyblr#medblr#scientific illustration
2 notes
·
View notes
Photo

Organisation histologique des léiomyocytes
Les léiomyocytes sont des cellules musculaires dont les protéines contractiles ne sont pas organisées sous forme de myofibrilles, ce qui leurs donnent au microscope optique un aspect non strié mais lisse : c'est pourquoi on parle aussi de cellules musculaires lisses. Leur contraction est à chaque fois involontaire et on les retrouve du coup dans beaucoup de viscères.
Histologiquement, ces cellules baignent dans un tissu conjonctif peu abondant, contenant des fibres de réticuline (autrement dit du collagène de type III comme autours de tout les autres types de cellules musculaires), de collagène de type I, des fibres élastiques pour que le tissu reprenne sa forme initiale après déformation, des nerfs du système nerveux autonome, et des vaisseaux. On note aussi la présence d'une lame basale autours des léiomyocytes, autre point commun avec la matrice extra-cellulaire des autres types de muscles.
Ces schémas ont été faits pour mes ED du Tutorat à partir des cours que j'ai retranscrit quand j'étais en première année de médecine. Ma seule source est le professeur de l'époque, et je peux avoir mal compris certaines choses, faire des approximations fausses, etc même si je fais de mon mieux. Croiser les sources permet d'avoir des informations plus fiables. N'hésitez pas à commenter pour discuter des sujets abordés ! Schémas et explications faits entre 2015 et 2016.
#histologie#tissus musculaires#organisation histologique des leiomyocytes#medecine#paces#ue 2#biologie#science#corps humain#studyblr#medblr#scientific illustration
1 note
·
View note
Photo

Myofibroblaste
Les myofibroblastes, comme les péricytes, sont des cellules non musculaires capables de se contracter, et qui sont apparentées aux fibroblastes. Ce sont des cellules fusiformes et éosinophiles à cause de leur haute teneur en protéines contractiles, qui interviennent dans les processus de cicatrisation par exemple.
Il y a d'abord une différenciation de fibroblastes dans les tissus conjonctifs autours de la lésion en myofibroblastes, qui se mettent ensuite en réseau de part et d'autre de la brèche. Ils vont alors sécréter de la matrice extra-cellulaire (MEC) pour combler la brèche, et se contracter pour en rapprocher les berges. Lorsque le tissu est cicatrisé, les myofibroblastes entrent en apoptose pour pas qu'il y ait un surplus de cellules ou de tissu néo-synthétisé en excès.
Ces schémas ont été faits pour mes ED du Tutorat à partir des cours que j'ai retranscrit quand j'étais en première année de médecine. Ma seule source est le professeur de l'époque, et je peux avoir mal compris certaines choses, faire des approximations fausses, etc même si je fais de mon mieux. Croiser les sources permet d'avoir des informations plus fiables. N'hésitez pas à commenter pour discuter des sujets abordés ! Schémas et explications faits entre 2015 et 2016.
#histologie#tissus conjonctifs#myofibroblaste#medecine#paces#ue 2#biologie#science#corps humain#studyblr#medblr#scientific illustration
1 note
·
View note
Photo

Muscle lisse multi-unitaire
Les léiomyocytes sont des cellules musculaires dont les protéines contractiles ne sont pas organisées sous forme de myofibrilles, ce qui leurs donnent au microscope optique un aspect non strié mais lisse : c'est pourquoi on parle aussi de cellules musculaires lisses. Ils peuvent être regroupés dans les tissus de façon unitaire ou multi-unitaire selon les relations entre les cellules.
Dans les muscles lisses multi-unitaires, la lame basale (un isolant électrique) est continue et sépare les léiomyocytes, de façon à ce que chacun soit dépolarisé séparément. Ainsi chaque léiomyocyte peut être contracté (jaune) individuellement par une stimulation nerveuse locale. Cela forme des foyers de contraction indépendants autours des varicosités, renflements axonaux du système nerveux autonome qui commande involontairement ces muscles (on les retrouve aussi dans les cardiomyocytes avec un rôle de régulation). Les muscles lisses multi-unitaires sont des structures qu'on retrouve à certains muscles lisses comme ceux qui entourent le canal déférent, l'iris ou la prostate.
Ces schémas ont été faits pour mes ED du Tutorat à partir des cours que j'ai retranscrit quand j'étais en première année de médecine. Ma seule source est le professeur de l'époque, et je peux avoir mal compris certaines choses, faire des approximations fausses, etc même si je fais de mon mieux. Croiser les sources permet d'avoir des informations plus fiables. N'hésitez pas à commenter pour discuter des sujets abordés ! Schémas et explications faits entre 2015 et 2016.
#histologie#tissus musculaires#muscle lisse multi-unitaire#medecine#paces#ue#biologie#science#corps humain#studyblr#medblr#scientific illustration
0 notes